Väterliche Kontrolle in neuronalen Stammzellen
Forscher zeigen erstmals, wie der väterlich geprägte genetische Faktor Zac1 die Entwicklung von neuronalen Stammzellen kontrolliert
Bei der Entstehung jedes Menschen findet im Mutterleib eine Art „genetisches Tauziehen“ statt. Während väterliche Gene daran interessiert sind, möglichst viele Ressourcen aus der Mutter herauszuholen, versucht das mütterliche Genom, den Organismus der Mutter vor zu starker Belastung zu schützen. Forscher am Max-Planck-Institut für Psychiatrie sind der Erklärung dieses elterlichen Gen-Konflikts für die Gehirnentwicklung einen wichtigen Schritt näher gekommen. Anhand von Stammzellen und Untersuchungen an Mäusen zeigen sie erstmals, wie der väterliche Faktor Zac1 die Differenzierung von neuronalen Stammzellen in Astrogliazellen entscheidend hemmt oder fördert.
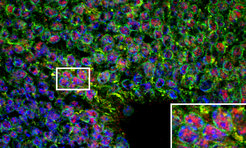
Damit aus einem anfangs kleinen Zellhaufen ein so hochkomplexes Organ wie das Gehirn entstehen kann, müssen Millionen Stammzellen sich entlang eines genetisch festgelegten Plans gezielt zu Nerven- oder Gliazellen entwickeln. Gliazellen werden auch als Unterstützerzellen bezeichnet, von denen eine Art, die Astrogliazellen, als die Stützstruktur für Neuronen dient und diese ernährt.
„Mit unserer jetzigen Studie konnten wir erstmals im Detail zeigen, wie Zac1 in differenzierenden neuronalen Stammzellen aktiviert ist und während der Entwicklung von Astrogliazellen Socs3 induziert“, erklärt Udo Schmidt-Edelkraut, Erstautor der Studie. Obwohl der Effekt von geprägten Genen auf die Gehirnentwicklung bereits allgemein bekannt war, ist der dahinterliegende zelluläre Mechanismus noch weitgehend unbekannt.
Das Zac1-Gen ist nur auf dem väterlichen Chromosom der DNA aktiv und kodiert das gleichnamige Zac1 Protein, das die Differenzierung von Astrogliazellen über einen indirekten Regelmechanismus kontrolliert. Dazu bindet es an mehreren Stellen der DNA und steuert die Bildung eines weiteren Proteins – des Socs3. Dieses Socs3 hat die Aufgabe, die Umwandlung von neuronalen Stammzellen in Unterstützerzellen zu hemmen, was für das Gehirn eine Notwendigkeit ist. Kommt es zu einem Verlust des Zac1, so fehlt diese genetische „Bremse“, Astrogliazellen bilden sich vermehrt und relativ unkontrolliert, was zu einer gestörten Ausbildung des neuronalen Netzwerks führen kann.
„Unsere Ergebnisse haben einen möglichen zellulären Mechanismus für den unterschiedlichen Einfluss elterlicher Genome auf spätere Gehirnerkrankungen aufgezeigt“, sagt Udo Schmidt-Edelkraut.
Wie bei allen höheren Lebewesen sind auch beim Menschen die väterlichen und mütterlichen Hälften des doppelten Chromosomensatzes nicht identisch, sondern unterscheiden sich funktionell. Typischerweise sind beide Kopien der insgesamt 25.000 menschlichen Gene aktiv. Doch bei 100-200 der Gene trifft dies nur auf die väterliche oder die mütterliche Kopie zu. Diese werden, je nachdem welche Kopie aktiv ist, als mütterlich oder väterlich geprägt bezeichnet. Ursache für die Prägung sind DNA-Methylierungen, die zur An- oder Abschaltung von Genen führen.
„Geprägte Gene sind wichtig für die embryonale Entwicklung und die Physiologie“, erklärt Udo Schmidt-Edelkraut. So könne ein Verlust der Prägung häufig zu schweren Fehlfunktionen des Stoffwechsels oder der Gehirnfunktionen führen. Beispiele sind frühkindliche Diabetes oder das Angelman-Syndrom, bei dem es häufig zu kognitiven Behinderungen, Hyperaktivität oder Konzentrationsschwierigkeiten kommt.
Für ihre Studie untersuchten die Forscher Zellkulturen von Mäusen und Menschen und verglichen diese miteinander. Aus ihren Daten schlussfolgerten sie, dass Socs3 sowohl im Menschen als auch in der Maus eine direkte Zielstruktur von Zac1 sei. Socs3 wurde über genomweite Expressionsprofilierung in neuronalen Stammzellen als Zielgen von Zac1 isoliert.
MG
