Körper und Psyche: Zwei Seiten einer Medaille
Forschungsbericht (importiert) 2019 - Max Planck Institut für Psychiatrie
Stressinduzierte Erkrankungen gehören zu den häufigsten gesundheitlichen Problemen weltweit. Sie umfassen sowohl psychische Störungen, wie Depression, als auch körperliche Leiden, wie Diabetes. Diese Krankheitsbilder stehen in einem kausalen Zusammenhang zueinander, und die Mechanismen der Stressregulation könnten eine gemeinsame Ursache körperlicher und psychischer Störungen sein. Wir konnten einen zentralen Mechanismus identifizieren, der entscheidend an der Entstehung stressinduzierter Erkrankungen beteiligt ist und einen neuen Ansatz zur Behandlung darstellt.
Einleitung
Stresserfahrungen nehmen in unserer modernen Gesellschaft eine zentrale Rolle ein und haben einen dramatischen Einfluss auf unser Leben und unsere Gesundheit. Vor allem die Art der Stressoren und deren mögliche Kontrollierbarkeit haben sich grundsätzlich verändert und die meisten Menschen müssen mit einem hohen Maß an Unwägbarkeiten und Planungsunsicherheit zurechtkommen. Die daraus resultierenden Belastungen führen immer häufiger zu einer Überlastung und physiologischer sowie psychologischer Erschöpfung. Die Weltgesundheitsorganisation (WHO) schätzt, dass die weltweit am meisten als belastend eingestuften Erkrankungen allesamt durch Stress ausgelöst beziehungsweise verstärkt werden, so dass mindestens ein Drittel der gesellschaftlichen Krankheitsbelastung auf Stress zurückzuführen ist [1].
Stresserfahrungen beeinflussen den ganzen Körper
Stress ist einer der Hauptrisikofaktoren für psychiatrische Erkrankungen wie zum Beispiel Depression oder Posttraumatische Belastungsstörung. In der Europäischen Union leiden jährlich mehr als 160 Millionen Menschen an psychiatrischen Erkrankungen, deren Behandlung als eine der größten Herausforderungen des 21. Jahrhunderts gilt. Gleichzeitig ist Stress auch ein wichtiger Risikofaktor für metabolische Erkrankungen wie Übergewicht und Typ 2 Diabetes. Auch hier gibt es einen weltweiten, epidemieartigen Anstieg der Erkrankungen zu verzeichnen. So leiden aktuell 650 Millionen Menschen weltweit an den Folgen von Fettleibigkeit und 422 Millionen Menschen an Diabetes. Interessanterweise gibt es einen fundamentalen Zusammenhang zwischen metabolischen und psychiatrischen Erkrankungen. So leiden Patienten mit einer Depression deutlich häufiger auch zusätzlich an metabolischen Erkrankungen, während auch die Prävalenz von psychiatrischen Erkrankungen wie der Depression unter Diabetespatienten deutlich erhöht ist [2]. Dementsprechend ist es enorm wichtig, die gemeinsamen molekularen Mechanismen zu erforschen, die stressinduzierten psychiatrischen und metabolischen Erkrankungen zugrunde liegen.
Das Protein FKBP51 ist ein Schlüsselregulator der körperlichen Stressantwort
Das Protein FKBP51 aus der Familie der FK-Bindungsproteine spielt eine zentrale Rolle bei der Regulation der Stresshormonausschüttung. FKBP51 ist, zusammen mit dem Protein HSP90, ein wichtiger Bestandteil des Protein-Komplexes des Glukokortikoidrezeptors (GR). Eine hohe FKBP51-Konzentration führt zu einer verminderten GR-Sensitivität für das Stresshormon Cortisol. Dies führt zum einen zu einer geringeren negativen Rückkopplung bei der Stressregulation und letztendlich zu einer erhöhten Aktivität der Stresshormonkaskade. Zum anderen wird FKBP51 selbst stressabhängig reguliert und beeinflusst eine Reihe von intrazellulären Signalkaskaden.
Aufgrund dieser zentralen Rolle in der Vermittlung der Stressreaktion ist es nicht verwunderlich, dass DNA-Sequenzvarianten in den regulatorischen Regionen des FKBP51-Gens zu einer erhöhten Wahrscheinlichkeit für stressbedingte Erkrankungen beitragen. So führt eine solche FKBP51-Variante vor allem dann zu einem vermehrten Auftreten von Depression und posttraumatischer Belastungsstörung, wenn Träger der Risikovariante starken Stresserfahrungen ausgesetzt waren [3]. Gleichzeitig sind diese FKBP51-Sequenzvarianten auch mit metabolischen Erkrankungen wie Fettleibigkeit und Typ 2 Diabetes assoziiert. Unser Forscherteam konnte nun Mechanismen entschlüsseln, die den unterschiedlichen FKBP51-vermittelten Erkrankungsbildern zu Grunde liegen.
FKBP51-Inhibitoren haben weitreichendes Potential bei der Behandlung von stressinduzierten Erkrankungen
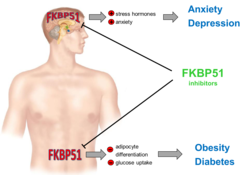
Durch die Entwicklung der ersten hochselektiven FKBP51-Inhibitoren konnte in ersten Machbarkeitsstudien die Effektivität einer FKBP51-basierten Behandlung nachgewiesen werden [4] . Im Gehirn wirken sie angstlösend und könnten damit vor allem bei der Behandlung stressinduzierter Angsterkrankungen wirksam sein. Auf der anderen Seite führt eine Verminderung von FKBP51 in Muskelzellen über einen Mechanismus in der Insulin-Signalkaskade zu einer verbesserten Glukosetoleranz und wirkt damit antidiabetisch. Auch im Fettgewebe scheint FKBP51 eine wichtige Rolle zu spielen und könnte hier durch die Induktion von beigen Fettzellen zu einer erhöhten Energiestoffwechselrate führen. Eine Behandlung von fettleibigen Mäusen mit einem FKBP51-Inhibitor führte dementsprechend zu einer Normalisierung der Glukosetoleranz und gleichzeitig zu einem signifikanten Gewichtsverlust [5]. Damit könnten vor allem peripher wirkende FKBP51-Inhibitoren ideal zur Behandlung von Hochrisikopatienten mit Diabetes in Kombination mit Adipositas eingesetzt werden.
Ausblick
Die bisherigen Ergebnisse sind sehr vielversprechend und bieten durch einen neuartigen Wirkmechanismus ganz neue Therapiemöglichkeiten für stressbedingte psychiatrische und metabolische Erkrankungen. Die hochselektiven, niedermolekularen FKBP51-Inhibitoren bieten einen exzellenten Ausgangspunkt für die weitere Entwicklung. Vor allem die Erforschung der Effekte von nicht-hirngängigen FKBP51-Inhibitoren für die Behandlung von Fettleibigkeit und Diabetes soll in den nächsten Jahren vorangetrieben werden, um in einigen Jahren zusammen mit Industriepartnern erste klinische Studien zu ermöglichen.
Literaturhinweise
Diabetes Care 31, 2383–2390 (2008)
Nature Neuroscience 16, 33–41 (2013)
